Ein neu entwickelter Nanobody könnte die Behandlung der Mukoviszidose (Cystische Fibrose, CF) grundlegend erweitern. Forschenden der Charité – Universitätsmedizin Berlin und des Leibniz-Forschungsinstituts für Molekulare Pharmakologie (FMP) ist es erstmals gelungen, einen zellgängigen Antikörperbaustein zu entwickeln, der direkt im Zellinneren ansetzt und den bei Mukoviszidose häufig defekten CFTR-Kanal stabilisiert und funktionell verbessert. Die Ergebnisse wurden im Fachjournal Nature Chemical Biology veröffentlicht.
Mukoviszidose wird in den meisten Fällen durch die sogenannte F508del-Mutation im CFTR-Gen verursacht. Diese führt dazu, dass der CFTR-Kanal fehlgefaltet ist und vorzeitig in der Zelle abgebaut wird. Infolgedessen wird der Wasser- und Salztransport gestört, und es bildet sich zäher Schleim in der Lunge, der chronische Infektionen und Entzündungen begünstigt.
Moderne CFTR-Modulatoren – insbesondere die Dreifachtherapie aus Elexacaftor, Tezacaftor und Ivacaftor – können die Funktion des Kanals bereits deutlich verbessern. Dennoch sprechen nicht alle Patient:innen ausreichend auf diese Therapie an, und eine vollständige Wiederherstellung der Funktion wird meist nicht erreicht.
Der nun entwickelte Nanobody setzt direkt an der Ursache an: Er bindet an das fehlgefaltete CFTR-Protein im Zellinneren und unterstützt dessen korrekte Faltung. Mithilfe sogenannter zellpenetrierender Peptide kann der Antikörperbaustein in die betroffenen Zellen der Atemwege gelangen.
In Zellmodellen von Mukoviszidose-Patient:innen zeigte sich, dass der Nanobody den defekten Kanal stabilisiert und dessen Funktion wiederherstellen kann. In Kombination mit der etablierten Dreifachtherapie ergab sich ein deutlicher Synergieeffekt: Die CFTR-Aktivität konnte in den Experimenten auf bis zu etwa 90 Prozent des Normalniveaus gesteigert werden.
„Durch diesen neuen Wirkmechanismus lässt sich die CFTR-Funktion in Kombination mit bestehenden Modulatoren deutlich besser korrigieren“, erklärt Marcus Mall, DZL-Wissenschaftler und Direktor der Klinik für Pädiatrie mit Schwerpunkt Pneumologie, Immunologie und Intensivmedizin an der Charité. „Unsere Ergebnisse deuten darauf hin, dass perspektivisch sogar eine weitgehende Normalisierung möglich sein könnte.“
Bis zu einer klinischen Anwendung sind jedoch weitere Forschungsarbeiten notwendig. Dazu zählen insbesondere die Entwicklung geeigneter inhalativer Verabreichungsformen sowie Untersuchungen zur Wirkung im menschlichen Körper und zur Immunverträglichkeit.
Der Ansatz könnte zudem über die Mukoviszidose hinaus relevant sein: Intrazelluläre Nanobody-Therapien bieten grundsätzlich neue Möglichkeiten zur Behandlung von Erkrankungen, die durch fehlgefaltete Proteine verursacht werden.
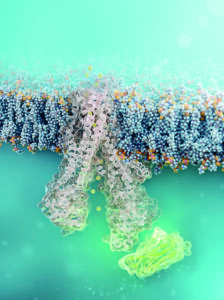
Zellgängiger Nanobody (grün) bindet an defekten CFTR-Chloridkanal (strukturelle Simulation) © FMP | Barth van Rossum
Originalpublikation: Franz L, Rubil T, Balázs A, Overtus M, Kemnitz-Hassanin K, Govaerts C, Mall MA, Hackenberger CPR. A cell-permeable nanobody to restore F508del cystic fibrosis transmembrane conductance regulator activity. Nat Chem Biol. 2026 Apr 17. doi: 10.1038/s41589-026-02199-w. Epub ahead of print. PMID: 41998105.